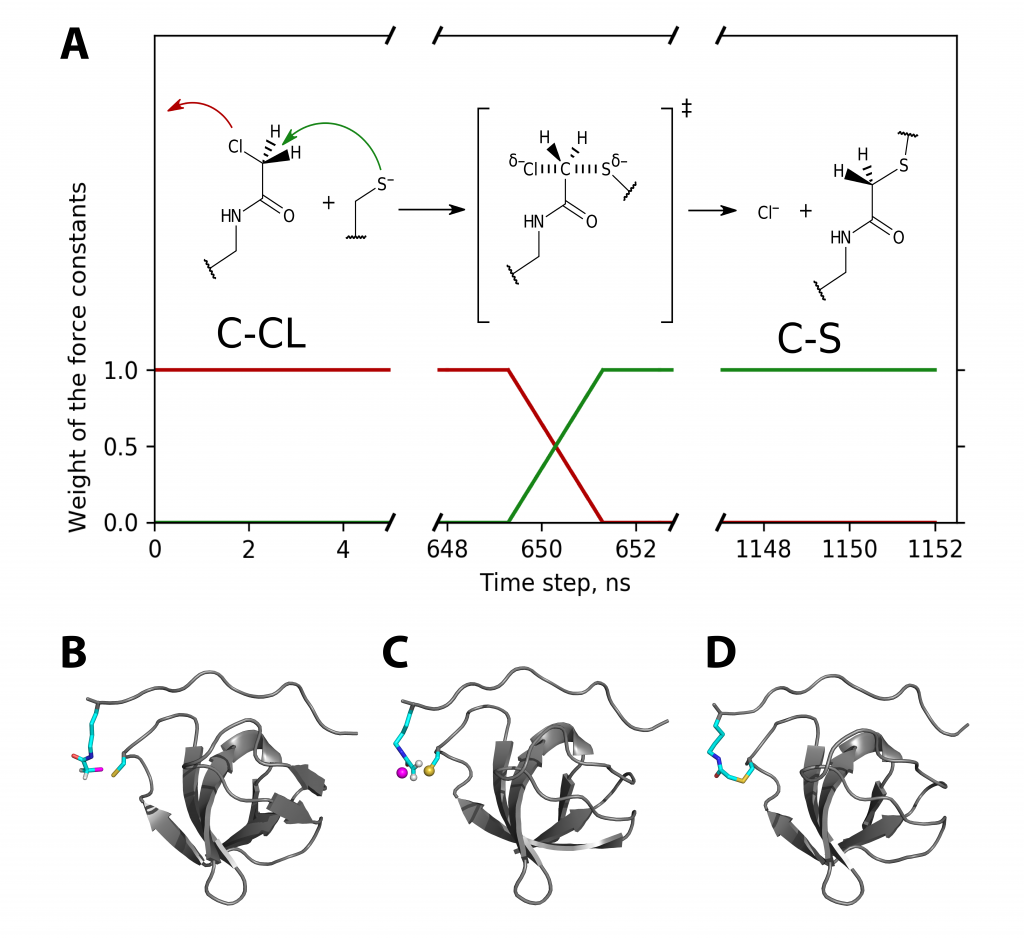
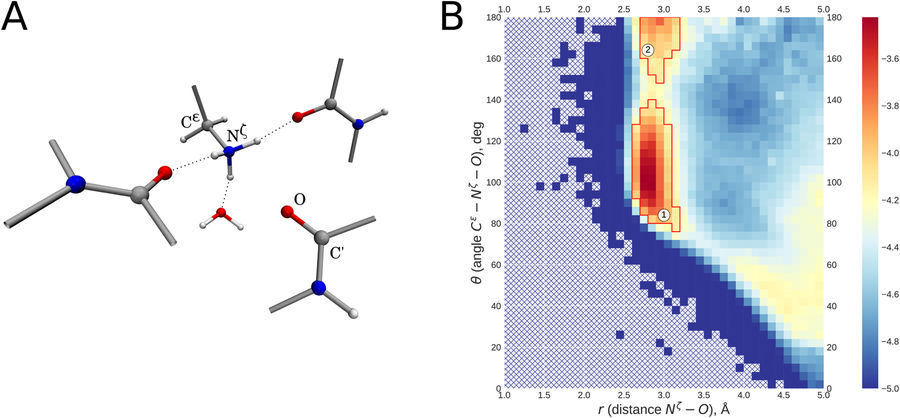
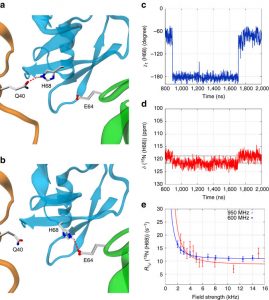
О лаборатории биомолекулярного ЯМР СПбГУ были опубликованы две статьи в журнале “Санкт-Петербургский университет” №4 (3930) 31 июня 2021.
В первой статье мы рассказали журналистам о новом способе распознавания спектральных сигналов амилоидных фибрилл, который поможет лучше разобраться в механизме нейродегенеративных заболеваний.
Во второй статье мы рассказали журналистам о лаборатории, целях, задачах и планах на будущее. Лаборатории биомолекулярного ЯМР СПбГУ почти восемь лет.
Tags: Измайлов, Лебеденко, Лузик, Михайловский, Подкорытов, Рогачева, Саликов, Скрынников, Харьков